ANÁLISIS INTEGRAL DEL DESEMPEÑO DE FOTOCATALIZADORES EN LA PRODUCCIÓN DE HIDRÓGENO
Leticia M. Torres-Martínez*
CIENCIA UANL / AÑO 23, No.100 marzo-abril 2020
DOI: https://doi.org/10.29105/cienciauanl23.100-1
RESUMEN
Se presenta una revisión y análisis integral de resultados de NaTaO3 (perovskita) y la solución sólida Na2ZrxTi6-xO13 (x = 0,1) de túneles rectangulares, en forma de polvos y películas, con alto desempeño en la producción foto y electrocatalítica de H2. La eficiencia de estos procesos fue mejorada mediante: a) el estudio del efecto del método de síntesis en las propiedades y su desempeño en estos procesos, b) la construcción de microestructuras facetadas en películas delgadas, y c) la formación de heteroestructuras mediante el depósito de cocatalizadores metálicos. Se obtuvieron películas delgadas del NaTaO3 con estructura tipo perovskita, altamente cristalinas por LCVD sobre sustratos de acero inoxidable para su aplicación en la reacción fotocatalítica de conversión de agua. Se logró el depósito de películas delgadas de la fase ortorrómbica NaTaO3, mediante la técnica de LCVD, con microestructura altamente facetada tipo piramidal; se observó, además, la presencia de nanoescalones. La eficiencia de las películas de LCVD-NaTaO3 fue 13 veces superior a la de los polvos. Se prepararon exitosamente nanobastones 1D, de las fases Na2ZrxTi6-xO13 (x = 0,1) con estructura de túneles rectangulares, mediante el método de solvocombustión.
Palabras clave: NaTaO3, Na2ZrxTi6-xO13 (x = 0,1), foto(y electro)catálisis, hidrógeno, heteroestructuras.
ABSTRACT
This article presents a revision and integral analysis of the results obtained from NaTaO3 (perovskite) and solid solution of Na2ZrxTi6-xO13 (x =0,1) of rectangular tunnels, in powder and film form, with high performance in the production of photo(and electro)catalysis of H2. The efficiency of these processes was enhanced through: a) the study of the effect of the synthesis methods in the performance and properties of these processes, b) the construction of faceted microstructures in thin films, and c) the formation of heterostructures through the deposition of metallic cocatalysts. Thin films of NaTaO3 with perovskite structures were obtained highly crystalline by LCVD over stainless steel substrates, for its application in the photocatalytic reaction of water conversion. Orthorhombic phase thin films of NaTaO3 was obtained by LCVD, with highly piramidal faceted microstructure; it was also observed the presence of nanosteps. The efficiency of the LCVD films of NaTaO3 was 13 times higher than other powders. 1D Nanotubes were successfully prepared, from the phases Na2ZrxTi6-xO13 (x=0,1) with rectangular tunnels structures, through the method of solvocombustion.
Keywords: NaTaO3 ; Na2ZrxTi6-xO13 (x = 0,1), Photo(and electro)catalysis, Hydrogen, Heterostructures.
El incremento en la demanda de energía, aunado al excesivo uso de los combustibles fósiles y las respectivas consecuencias ambientales, ha motivado la utilización de nuevas fuentes de energía. Los desarrollos tecnológicos de estas fuentes requieren ser sustentables y accesibles en costo, pues comúnmente la generación de energía produce gases de invernadero y otros contaminantes. Entre las diversas fuentes de energía renovable destaca la energía solar. En una hora llega a la Tierra más energía del Sol que toda la energía consumida por la sociedad en un año. En este sentido, el desarrollo de fuentes renovables de energía que sean amigables con el medio ambiente se ha convertido en un tema de atención prioritaria en los últimos cuarenta años (Bartels, Pate y Olson, 2010). Entre las alternativas desarrolladas para el aprovechamiento de la energía solar se encuentran las basadas en procesos fotovoltaicos y fotocatalíticos. En particular, la fotocatálisis se ha consolidado como uno de los procesos más prometedores, con mayor impacto científico, tecnológico y económico para la sociedad debido a las ventajas que involucra, como operación a temperatura y presión ambiental, alta selectividad y reproducibilidad, además de la factibilidad de su escalamiento a nivel industrial (Wan et al., 2018). El alcance de sus aplicaciones comprende desde los ya conocidos procesos de remediación ambiental, hasta la novedosa generación de combustibles limpios a partir de fuentes abundantes, como agua, dióxido de carbono y energía solar (Zeng et al., 2018).
De esta manera, la investigación en el área de la fotocatálisis emerge como una de las herramientas más fuertes para hacer frente a los retos ambientales y energéticos del siglo XXI. En particular, los sistemas energéticos basados en la utilización del hidrógeno representan una de las mejores alternativas debido a su alta eficiencia, compatibilidad ambiental y versatilidad. Además de ser renovables, el principio básico de generar energía a partir del hidrógeno es combinarlo con el oxígeno utilizando celdas de combustible, para generar electricidad y atender todo tipo de demandas (Winter, 2009). El proceso de conversión fotoinducida del agua en H2 y O2 mediante el uso de materiales fotocatalizadores y radiación solar se ha empleado eficientemente en sistemas fotocatalíticos o de celdas fotoelectroquímicas (HPC y PEC) (Krol y Parkinson, 2017). El desarrollo de estas tecnologías para su uso en gran escala posee un gran atractivo debido a que el hidrógeno constituye un vector energético que no genera contaminantes tras su uso, además de poseer alta densidad energética. Esta reacción ha recibido mucha atención debido a su factibilidad para el abastecimiento de la demanda futura de combustibles alternos y limpios, para la industria química y las aplicaciones relacionadas con la energía. Sin embargo, su aplicación a mayor escala sigue estando limitada por las bajas eficiencias alcanzadas. En este sentido, uno de los mayores retos en este campo de investigación es el diseño y preparación de materiales fotocatalizadores sustentables, eficientes y abundantes que sean capaces de llevar a cabo la generación de hidrógeno a partir de la luz solar.
Para lograr una economía basada en el hidrógeno, es necesario tener fotocatalizadores eficientes, estables y baratos con la capacidad de producir hidrógeno cuando son iluminados por la luz solar. Los requerimientos básicos de los catalizadores no son simples, entre éstos se incluyen: absorción de la luz en la región del visible, estabilidad en solución acuosa, y un potencial adecuado de sus bandas de valencia y conducción en comparación con los potenciales redox del agua (Li et al., 2018). Entre las familias de materiales que presentan estas propiedades para su uso en procesos fotoinducidos y otras diversas aplicaciones, se encuentran los titanatos, tantalatos, vanadatos, niobatos, molibdatos, etcétera (Kudo, 2003; Jitputti et al., 2006). De los óxidos metálicos que han sido más investigados para la reacción de conversión del agua en H2 y O2 se destacan los formados por cationes con configuración electrónica d0 a d10 (Takata, Pan y Domen, 2015). Estos materiales pueden ser preparados mediante una gran diversidad de métodos, con estructuras cristalinas estables del tipo perovskitas, túneles rectangulares (1D) y esquelitas, entre otras (Zhu et al., 2014). Los tantalatos y titanatos han sido el tema central de múltiples investigaciones, dirigidas al estudio del efecto de la estructura cristalina, morfología, microestructura y tamaño de partícula sobre la eficiencia fotocatalítica (Lv et al., 2017). Sin embargo, son pocos los estudios que se enfocan en un análisis integral de los diversos factores más relevantes en el desempeño de los diferentes procesos fotoinducidos, en donde se incluyan, además, la influencia significativa que tienen las pequeñísimas variaciones tanto morfológicas como las cristaloquímicas de la microestructura cristalina.
En este trabajo se presenta un resumen del análisis integral de las propiedades estructurales, morfológicas, ópticas, texturales y de desempeño en la producción foto y electrocatalítica de hidrógeno de dos tipos de fotocatalizadores: con estructura tipo perovskita (ABO3: tantalato) y de túneles rectangulares, unidimensionales (1D: titanatos), preparados en forma de polvos y película delgada. El análisis de la evaluación se basó en la influencia de varios factores: a) el efecto del método de síntesis (LCVD: depósito químico en fase vapor asistido por láser, estado sólido, sol-gel, solvocombustión), b) la construcción de microestructuras altamente facetadas en películas delgadas preparadas por la técnica de LCVD, y c) la formación de heteroestructuras mediante el depósito de los cocatalizadores MO (M = Cu, Ni).
METODOLOGÍA EXPERIMENTAL
Depósito de películas nanoestructuradas por LCVD
Se prepararon películas de NaTaO3 con microestructuras altamente facetadas mediante la técnica de LCVD. Los precursores fueron calentados a su temperatura de volatilización. A través de un gas de arrastre, los precursores son transportados hasta la cámara en donde se llevó a cabo la reacción de formación de los productos, la cual es asistida por un láser. La temperatura de depósito se controla a través de la potencia del láser empleada. Como precursor de Na se empleó dipivaloilmetanato de Na, y como precursor de Ta se empleó isopropóxido de Ta. Los flujos de gas empleados de Ar y O2 gases fueron de 1.7×10-6 y 2.5×10-6 m3 s-1, respectivamente. La presión total en la cámara de depósito se mantuvo a 0.4 kPa. Se emplearon sustratos de acero inoxidable y se calculó la tasa de depósito a partir del espesor de las películas y el tiempo de depósito (10 min).
Síntesis de Na2Ti6O13 por estado sólido y sol-gel
El compuesto Na2Ti6O13 fue preparado por reacción del estado sólido y sol-gel. Por estado sólido se mezclaron estequiométricamente los precursores puros y secos: Na2CO3 (99.9% DEQ) y TiO2 (Degussa P25), BaCO3 (> 99% Sigma Aldrich), y Li2CO3 (99% Fermont). Los materiales fueron tratados térmicamente en crisoles de platino hasta 800°C en atmósfera de aire. Para la síntesis por sol-gel del Na2Ti6O13 se disolvió butóxido de titanio (97% Sigma Aldrich) en etanol anhidro. En otro recipiente se disolvió acetato de sodio (99.9% Fermont) en agua y se agregó gota a gota a la primera solución. Los geles obtenidos se trataron térmicamente a 900°C para completar la formación de las fases.
Síntesis de Na2ZrxTi6-xO13 (x = 0, 1) por solvocombustión
Se usaron como precursores butóxido de titanio (97% Aldrich), acetato de sodio anhidro, (99% Aldrich) y butóxido de zirconio (80% Aldrich) para preparar las fases Na2ZrxTi6-xO13 (x = 0,1). Se mezclaron cantidades estequiométricas de los reactivos en un matraz con 30 ml de acetilacetona-etanol (1:1). La mezcla se mantuvo bajo agitación y reflujo a 70°C hasta la evaporación completa de la solución. Después se transfirió el matraz a una parrilla precalentada a 180°C, donde se llevó a cabo la reacción de combustión.
Depósito de MO (M = Cu, Ni) como cocatalizadores por el método de impregnación por vía húmeda
Las partículas de óxidos metálicos fueron depositadas sobre los titanatos por el método de impregnación húmeda. Para esto, acetatos metálicos (acetato de cobre y de níquel) en diferentes proporciones (0.5-5% en peso) fueron disueltos en etanol. La fracción en masa correspondiente del fotocatalizador sintetizado se agregó, y la suspensión se mantuvo bajo agitación vigorosa durante una hora. Después de este tiempo, la temperatura se elevó a 80°C para lograr la completa evaporación del solvente y finalmente fueron tratados a 400°C durante dos horas para la formación del óxido.
Caracterización de los materiales
El análisis estructural de las muestras se llevó a cabo empleando un difractómetro de rayos X (DRX) modelo D8 Advance de la marca Bruker, el cual opera a 40 kV y 40 mA con radiación, CuKα (λ = 1.5406 Å) en un intervalo de 2θ de 10 a 70º y con un tamaño y tiempo de paso de 0.05° y 0.5 s, respectivamente. La morfología de los materiales se analizó con un microscopio electrónico de barrido (MEB-JEOL 6490LV) en el modo de electrones secundarios y alto vacío a 20 kV de voltaje. La cuantificación elemental de las muestras se realizó por espectroscopia de energía dispersiva de rayos X (EDX), analizando tres zonas al azar. También se llevaron a cabo análisis por microscopia electrónica de transmisión (MET) en un microscopio FEI-Titán con resolución de 0.7 Å. Las propiedades ópticas de las muestras se analizaron en un rango de 200-800 nm usando un espectrofotómetro UV-vis NIR Cary 5000, acoplado con una esfera de integración para mediciones de reflectancia difusa a través de las cuales se calculó la energía de banda prohibida de los materiales (Eg), usando la función Kubelka Munk. La caracterización fotoelectroquímica se llevó a cabo en un potenciostato-galvanostato (Metrohm Autolab), usando una celda de cuarzo convencional de tres electrodos (Ag/AgCl como electrodo de referencia, Pt como contraelectrodo y como electrodo de trabajo una película del material a analizar) y empleando una solución acuosa de Na2SO4 0.5 M como electrolito soporte. El área activa de los electrodos fue de 1 cm2 y la celda se iluminó con una lámpara de luz UV tipo pluma (UVP, 254 nm and 4,400 mW/cm2). Se realizaron análisis de fotocorriente (PC), voltamperometría lineal (VL) e impedancia electroquímica (EIS).
Evaluación de la actividad fotocatalítica de los materiales para la producción de hidrógeno
La actividad de los materiales se evaluó a temperatura ambiente en un reactor Pyrex de 250 mL. El fotocatalizador en polvo (0.2 g) o en película (5 mg) se colocó en un reactor con 200 ml de agua desionizada bajo agitación vigorosa. La solución se burbujeó con nitrógeno durante 30 min previo a la reacción. Entonces, la solución fue irradiada con una lámpara tipo pluma (UVP, 254 nm y 4,400 µW/cm2), y el hidrógeno producido se analizó en un cromatógrafo de gases Thermo Scientific conectado en línea y equipado con un detector de conductividad térmica (TCD) y una columna capilar de sílica fundida (30 m x 0.53 mm). Se empleó N2 como gas acarreador y se siguió la reacción durante 3 horas.
RESULTADOS Y DISCUSIÓN
Síntesis y caracterización estructural por DRX del NaTaO3
El NaTaO3 fue preparado en forma de película delgada mediante el depósito químico en fase vapor asistido por láser (LCVD). La figura 1 muestra el patrón de difracción de rayos X de las películas de (a) NaTaO3 ortorrómbico y (b) NaTaO3 monoclínico depositadas por LCVD. Estos patrones de DRX se indexaron con la fase ortorrómbica (Pcmn 62, a = 5.5213 Å, b = 7.7952 Å, y c = 5.4842 Å; JCPDS: 01-073-0878) y monoclínica (P2/m 10, a = 3.8995 Å, b = 3.8965 Å, y c = 3.8995 Å; JCPDS: 01-074-2479). Ambas películas exhibieron picos similares con diferente orientación preferencial. El NaTaO3 ortorrómbico exhibió una orientación preferencial en los planos (121) (002), mientras que el NaTaO3 monoclínico en los planos (100) (001). Otras diferencias se aprecian en el acercamiento en 2θ, ∼ en 68°, de tres a dos picos en las fases ortorrómbica y monoclínica del NaTaO3. Las diferencias en la orientación preferencial y estructura cristalina de las muestras fueron atribuidas a la variación de la temperatura de depósito del NaTaO3.
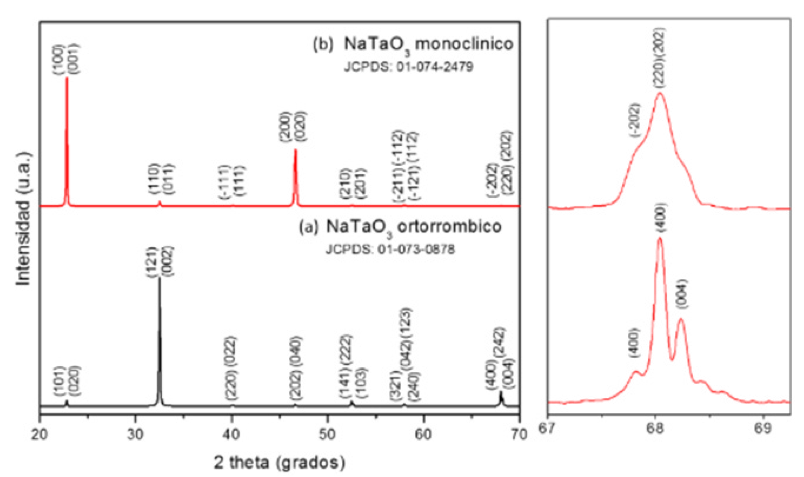
Figura 1. Patrones de difracción de rayos X de las películas de: (a) NaTaO3
ortorrómbico y (b) NaTaO3 monoclínico depositadas por LCVD.
Microscopia electrónica de barrido
La figura 2 muestra la microestructura superficial de las películas de (a) NaTaO3 ortorrómbico y (b) NaTaO3 monoclínico depositado sobre acero inoxidable por la técnica de LCVD. El NaTaO3 ortorrómbico exhibió una microestructura altamente facetada, en forma piramidal. La morfología observada en la película con NaTaO3 monoclínico presentó estructuras similares, pero de menor tamaño y no tan bien definidas como las primeras. La microestructura de un semiconductor juega un papel primordial en el desempeño fotocatalítico del material, ya que afecta directamente el proceso de separación de las cargas fotogeneradas (Van Winsen, 2013). La presencia de nanosteps (o nanoescalones) en la superficie de los materiales puede promover una separación efectiva de los pares electrón-hueco, debido a la presencia de caras cristalinas opuestas. Las caras cristalinas presentan diferente valor de carga superficial, por lo cual, el proceso de separación de cargas es optimizado en este tipo de estructura (Voorzanger, 2012). La absorción de la luz en el material también es influenciada por su microestructura (Osterloh, 2013), de este modo, la estructura piramidal obtenida en las películas de NaTaO3, así como la presencia de nanoescalones, promueve una mejor absorción de la luz y separación de cargas (figura 3c).

Figura 2. Microestructura superficial y vista transversal de las películas de (a) NaTaO3 ortorrómbico, (b) NaTaO3 monoclínico depositado por LCVD, y (c) mecanismo de separación de cargas en NaTaO3 ortorrómbico.
Propiedades ópticas de las películas determinadas por espectroscopia de reflectancia difusa
Las películas de NaTaO3 exhibieron absorción en la región UV, por debajo de los 320 nm. En el NaTaO3, la banda de conducción está compuesta principalmente por orbitales Ta5d; la banda de valencia, por orbitales O2p. En el espectro de absorción se pudo apreciar la transición banda a banda de los electrones desde los orbitales O2p a los orbitales Ta5d. Se construyeron las curvas Tauc para las películas de NaTaO3 (figura 3 a-b), considerando transiciones directas e indirectas para las fases ortorrómbica y monoclínica, respectivamente. NaTaO3 monoclínico exhibió la menor energía de banda prohibida (3.92 eV), comparado con NaTaO3 ortorrómbico (4.01 eV). Esto indica que los electrones fotogenerados en NaTaO3 ortorrómbico poseen mayor energía para llevar a cabo la reacción de reducción del agua. La estructura cristalina afecta directamente a la de bandas de los materiales y, por lo tanto, sus propiedades ópticas. En los tantalatos alcalinos con estructura tipo perovskita, se reporta la influencia del ángulo de enlace Ta-O-Ta en los octaedros sobre la deslocalización de energía, prediciendo una mejor deslocalización cuando el ángulo Ta-O-Ta es cercano a 180° (Eng et al., 2003). Este efecto se asocia con las diferencias en los valores del band gap de las fases ortorrómbica y monoclínica. A partir de este principio, se espera que la deslocalización de energía sea mayor en el NaTaO3 con estructura monoclínica. Sin embargo, también es bien sabido que el proceso de absorción de luz en un semiconductor con transición indirecta es menos eficiente que en un semiconductor con transición directa, debido a la implicación de una tercera partícula (fonón), lo cual reduce la eficiencia de absorción de la luz. Esto también afecta el espectro de absorción del semiconductor, promoviendo un salto más definido en el caso de un semiconductor con transición directa, comparado a aquéllos con transición indirecta (Kisch, 2015). Debido a que el NaTaO3 ortorrómbico presenta una transición directa, el proceso de absorción de la luz es más eficiente en este material, comparado con el NaTaO3 monoclínico, que exhibe una transición indirecta.
Caracterización fotoelectroquímica
La figura 4(a) presenta las curvas características de corriente-potencial de las películas de NaTaO3 depositadas por LCVD. La densidad de fotocorriente de las muestras a -0.8 V, así como los potenciales de circuito abierto y se resumen en la tabla I. A partir de las curvas presentadas en la figura 4(a), se determinó que los electrodos basados en las películas de NaTaO3 exhiben una mayor fotocorriente, en el rango de 4.3 (NaTaO3 ortorrómbico) a 4.1 (NaTaO3 monoclínico) mA/cm2. Los electrodos mostraron respuestas estables después de varios ciclos sin variación significativa en sus propiedades, confirmando la estabilidad para su uso en la reacción de descomposición del agua.
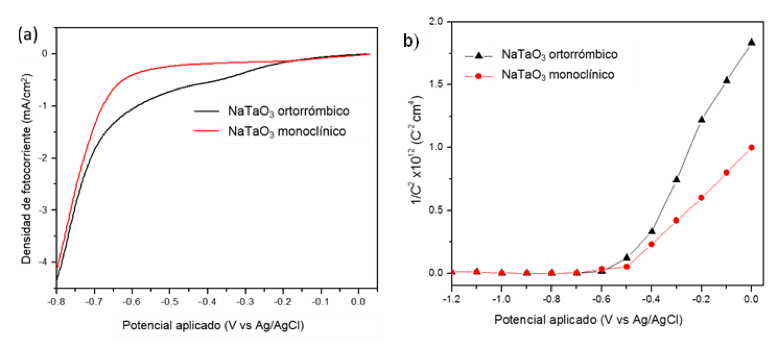
Figura 4. (a) Densidad de fotocorriente y (b) Mott Schottky de las películas de NaTaO3 depositadas por LCVD.
Las mediciones de espectroscopia de impedancia electroquímica permitieron investigar la transferencia de carga en los electrodos de NaTaO3. La figura 4(b) muestra las gráficas de Mott-Schottky de las películas de NaTaO3 preparadas por LCVD. El potencial de banda plana (flat band potential, EFB) y la densidad de donadores (Nd) se estimó a partir de estas curvas. Estos parámetros se resumen también en la tabla I. Las gráficas de Mott-Schottky de todas las muestras exhiben pendientes positivas, lo cual indica que los semiconductores son del tipo n. El potencial de banda plana de las muestras varía en el rango de -0.60 a -0.50 V. Este parámetro afecta directamente la fotorrespuesta del material, y un valor más negativo involucra una mejor habilidad para promover la separación de cargas en el semiconductor (Kumar et al., 2011). La densidad de donadores en los electrodos de NaTaO3 varió de 2.88×1012 a 1.10×1012 cm-3. Una densidad de donadores mayor implica una mayor concentración de portadores de carga, y está relacionada con una mayor conductividad en la muestra, y a un campo eléctrico más intenso en la interfaz semiconductor-electrolito, lo cual mejora la eficiencia del transporte de electrones y huecos en las regiones externas del electrodo, siendo esto favorable para su desempeño fotocatalítico (Cesar et al., 2009). La eficiencia de conversión se puede calcular en términos de la energía solar aprovechada en la producción de hidrógeno, a través de la siguiente ecuación:
η(%) = Jp [(1.23 – Vapp)/I0] x 100
donde Jp es la densidad de fotocorriente en mA/cm2, I0 es la intensidad de la luz incidente,
Vapp = Vmea – Voc
donde Vmea es el potencial del electrodo de trabajo al cual se midió la fotocorriente bajo iluminación y Voc es el potencial a circuito abierto bajo las mismas condiciones de trabajo (Kumar et al., 2011). La eficiencia de conversión más alta (%STH) se obtuvo en la película de NaTaO3 ortorrómbico (1.93 %), y corresponde con las propiedades más favorables para la reacción de water splitting, lo cual incluye una densidad de fotocorriente mayor, alta concentración de portadores de carga y una microestructura que promueve la separación y transferencia de las cargas fotogeneradas.
Producción fotocatalítica de hidrógeno del NaTaO3
La actividad fotocatalítica para la producción de H2 sobre las películas de NaTaO3 preparadas por LCVD se evaluó bajo luz UV y se presenta en la figura 5(a). Se observa que los fotocatalizadores exhibieron una actividad estable para la evolución de hidrógeno durante tres horas. No se observó disminución en la actividad, debido a la alta estabilidad de los materiales. La tasa promedio de producción de H2 se calculó a partir de estas curvas y los valores se presentan en la figura 5(b). Se calculó la actividad de los materiales en µmol.g-1h-1 para hacer una comparación con la actividad de los mismos materiales en polvo, y debido a que éstas son las unidades más comúnmente utilizadas para reportar la tasa de producción de H2. En el caso de películas, es importante comentar que la actividad de los fotocatalizadores se determinó por unidad de área superficial. El área superficial activa de los electrodos preparados en este trabajo es de 1 cm2 (Huerta-Flores et al., 2016; 2017).

Figura 5. (a) Producción de H2 en las películas de NaTaO3 preparadas por LCVD y (b) resumen de la actividad.
La tendencia presentada por los materiales en la tasa promedio de producción de hidrógeno fue: NaTaO3 ortorrómbico (74 µmol.cm-2) > NaTaO3 monoclínico (11 µmol.cm-2). En unidades de µmol.g-1h-1, la actividad de las muestras fue de 5672 y 888, respectivamente. La tasa de producción más alta se obtuvo por la película de NaTaO3 ortorrómbico, y corresponde al fotocatalizador que exhibió la eficiencia de conversión más alta calculada en la sección anterior (1.93% STH). Esta actividad se relaciona con las propiedades estructurales, ópticas, morfológicas y eléctricas de las películas. La mayor actividad obtenida por el NaTaO3 ortorrómbico se adjudicó a la morfología tipo piramidal y la presencia de nanoescalones por el uso de la técnica de depósito de LCVD. Este tipo de microestructura, en la cual caras cristalinas con diferente carga superficial crecen en sentido opuesto, promueve una separación eficiente de las cargas fotogeneradas y reduce la recombinación. Esta microestructura ofrece una mayor área superficial expuesta, y la presencia de escalones proporciona un mayor número de sitios activos para la reacción de evolución de hidrógeno. La absorción de luz en este fotocatalizador se favoreció por la naturaleza de su transición electrónica directa, en comparación a la transición indirecta en NaTaO3 monoclínico. Las mediciones fotoelectroquímicas presentadas corroboraron las propiedades superiores de la película de NaTaO3 ortorrómbico, lo cual se confirmó por la mayor densidad de fotocorriente observada, la mayor concentración de portadores de carga y la eficiencia de conversión más alta obtenida en esta muestra. La película de NaTaO3 ortorrómbico exhibió una actividad seis veces superior a la de la película de NaTaO3 monoclínico, y 13 veces mayor a la de NaTaO3 ortorrómbico obtenido en polvo por el método de solvocombustión (Gómez-Solís et al., 2014; Torres-Martínez et al., 2010).
Por otro lado, debido a que las fuentes de irradiación empleadas en los trabajos son diferentes, es difícil establecer una comparación directa de las actividades. Sin embargo, a través de la eficiencia de conversión calculada en las muestras desarrolladas en este trabajo, y la estimada en los trabajos previos, se estableció una comparación en términos del porcentaje de conversión de la energía solar usada en la producción de hidrógeno. Este parámetro es utilizado para describir la verdadera eficiencia de producción de hidrógeno en la reacción de descomposición del agua. Los valores de la eficiencia de conversión de las muestras preparadas por LCVD en este trabajo de revisión son significativamente mayores a las exhibidas por materiales similares preparados en polvo, y corresponden a eficiencias atractivas para el uso de estos materiales en reactores de mayor escala.
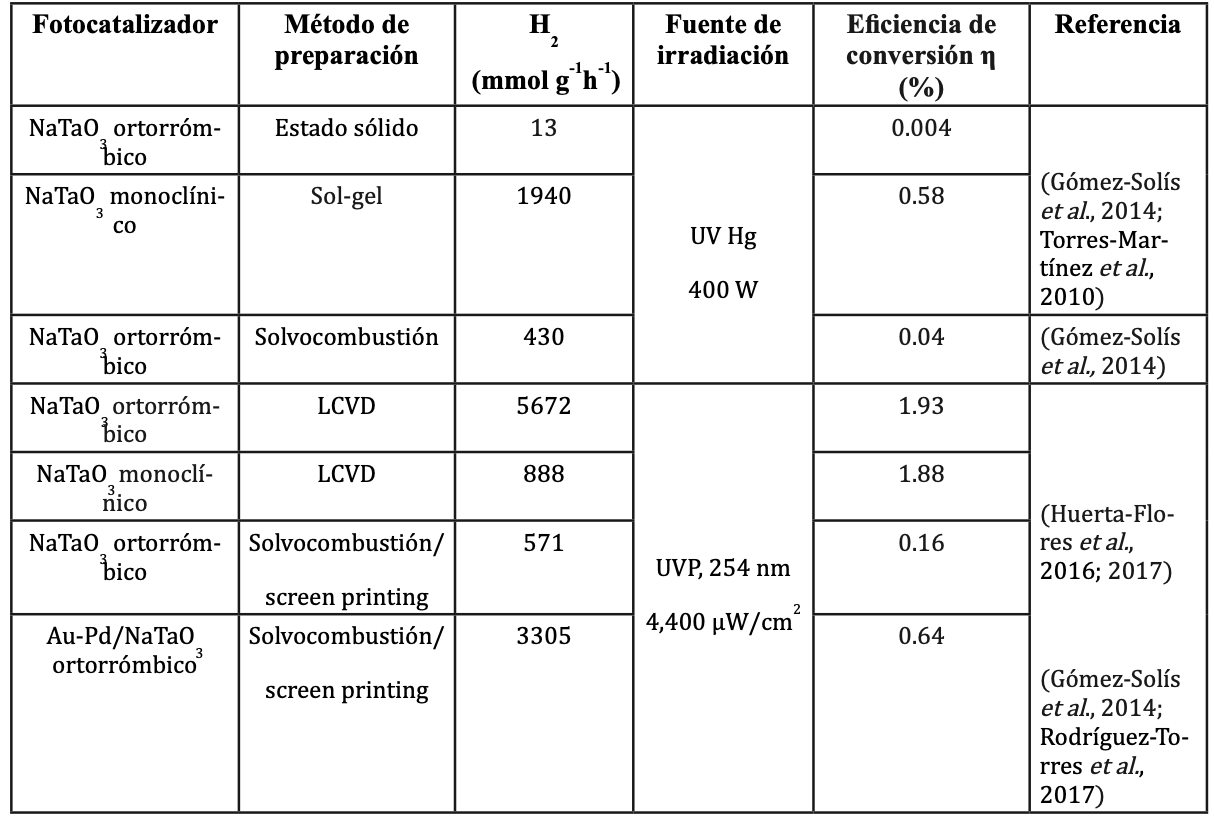
Tabla II. Resumen de las actividades en evolución de hidrógeno reportadas para NaTaO3 en sistemas fotocatalíticos.
Titanatos con estructura de túneles rectangulares: MO (M = Cu, Ni)/Na2ZrTi5O13 (x = 0.1)
Se presenta el análisis integral de los resultados de síntesis, caracterización y evaluación fotocatalítica para la producción de hidrógeno de los compuestos estudiados con estructura de túneles rectangulares y morfología unidimensional (1D) (Huerta-Flores, Torres-Martínez y Moctezuma, 2017).
Caracterización estructural y morfológica de la solución sólida Na2ZrxTi6-xO13 (x = 0,1)
La incorporación de un átomo de Zr en la estructura del Na2Ti6O13 fue evidenciada por DRX en polvos y refinando su patrón por el método Rietveld. En la tabla III se puede observar el desplazamiento de los parámetros de celda debido a la distorsión en los sitios octaédricos por la presencia del radio superior del Zr4+ (0.86 Å) comparado con el del Ti4+ (ri = 0.74 Å).
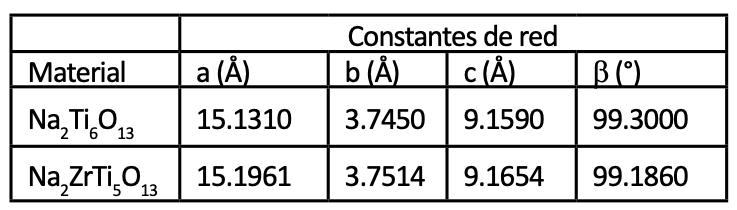
Tabla III. Parámetros cristalográficos obtenidos del refinamiento Rietveld de las muestras Na2Ti6O13 y Na2Ti5ZrO13.
.
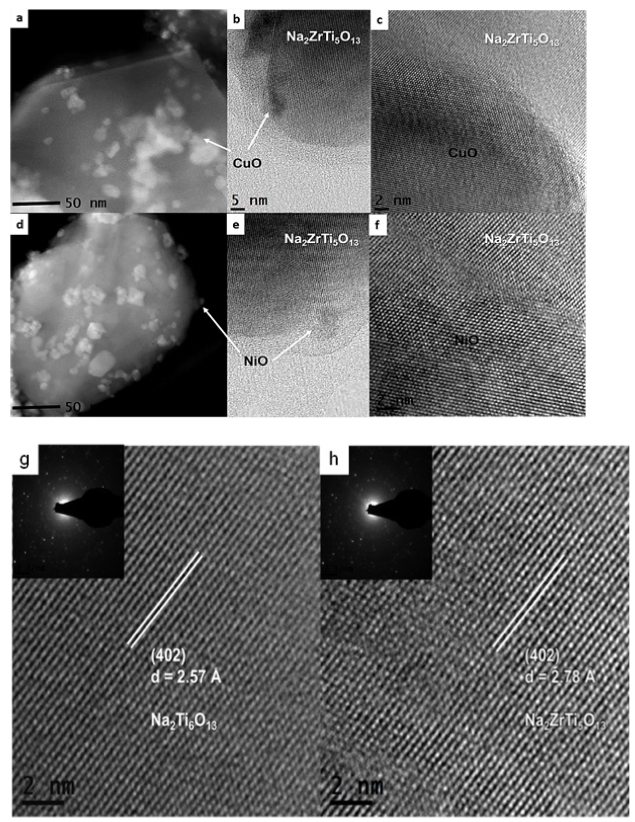
La morfología de las fases se estudió a través de microscopia electrónica de transmisión (figura 6). En estas imágenes se pueden observar las fases altamente cristalinas de Na2Ti6O13 y Na2ZrTi5O13, así como la dispersión homogénea de las nanopartículas de óxidos metálicos en la superficie de los materiales. A través de las imágenes MET de alta resolución de las muestras se calcularon las distancias interplanares, correspondiendo a 2.57 Å y 2.78 Å para el Na2Ti6O13 y el Na2ZrTi5O13, respectivamente, en el plano (402). Esto confirma la inserción del Zr4+ dentro de la estructura cristalina del Na2Ti6O13.
Producción fotocatalítica de las fases Na2ZrxTi6-xO13 (x = 0,1)
La actividad de las fases MO/Na2ZrxTi6-xO13 (x = 0,1) se resume en la figura 7. Como se observa en esta figura, la actividad del Na2Ti6O13 se incrementó 8.9 veces con la incorporación de Zr4+ en Na2ZrTi5O13. Esto se adjudicó a los siguientes factores: (i) debido a la diferencia en las longitudes de enlace Ti-O y Zr-O, y a la distribución de carga alrededor del dopante Zr, lo cual genera un campo eléctrico interno en la estructura, promoviendo una mejor separación de los electrones y huecos y mejorando la transferencia de carga en la fase Na2ZrTi5O13. Adicionalmente, (ii) los iones dopantes de Zr4+ pueden actuar como trampas de electrones. Estos electrones pueden ser transferidos a las moléculas de agua adsorbidas en la superficie del fotocatalizador. Este proceso disminuye la recombinación del par hueco-electrón, e incrementa la actividad fotocatalítica del material. La adición de nanopartículas de NiO y CuO como cocatalizadores también incrementó la actividad fotocatalítica, siendo la fase Na2ZrTi5O13-CuO el material que exhibió la mayor actividad, la cual corresponde a 13.6 veces la actividad del Na2Ti6O13 puro. De acuerdo a los resultados, se propone que los procesos de transferencia de carga optimizados en este material son consecuencia de la adecuada interdispersión del Na2ZrTi5O13 tipo n y el CuO tipo p, lo cual promueve un uso más eficiente de las cargas fotogeneradas, resultando en una mayor actividad fotocatalítica.
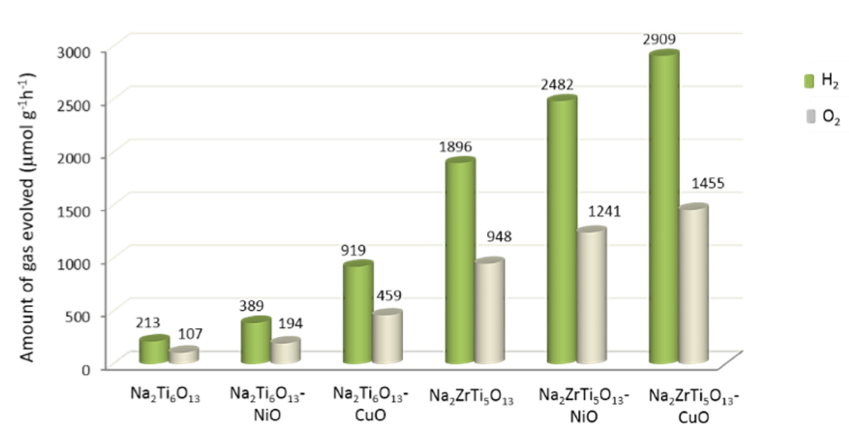
Figura 7. Resumen de la producción focatalítica de hidrógeno y oxígeno sobre las fases Na2ZrxTi6-xO13.
Es posible observar que la producción estequiométrica de hidrógeno y oxígeno sobre las fases MO-Na2ZrxTi6-xO13 (x = 0,1). Y también se puede inferir que es claro que las actividades obtenidas utilizando estos fotocatalizadores son superiores a la mostrada por fotocatalizadores similares, con la misma estructura unidimensional (1D) reportados en otros trabajos en la bibliografía, tal como se resume en la tabla IV
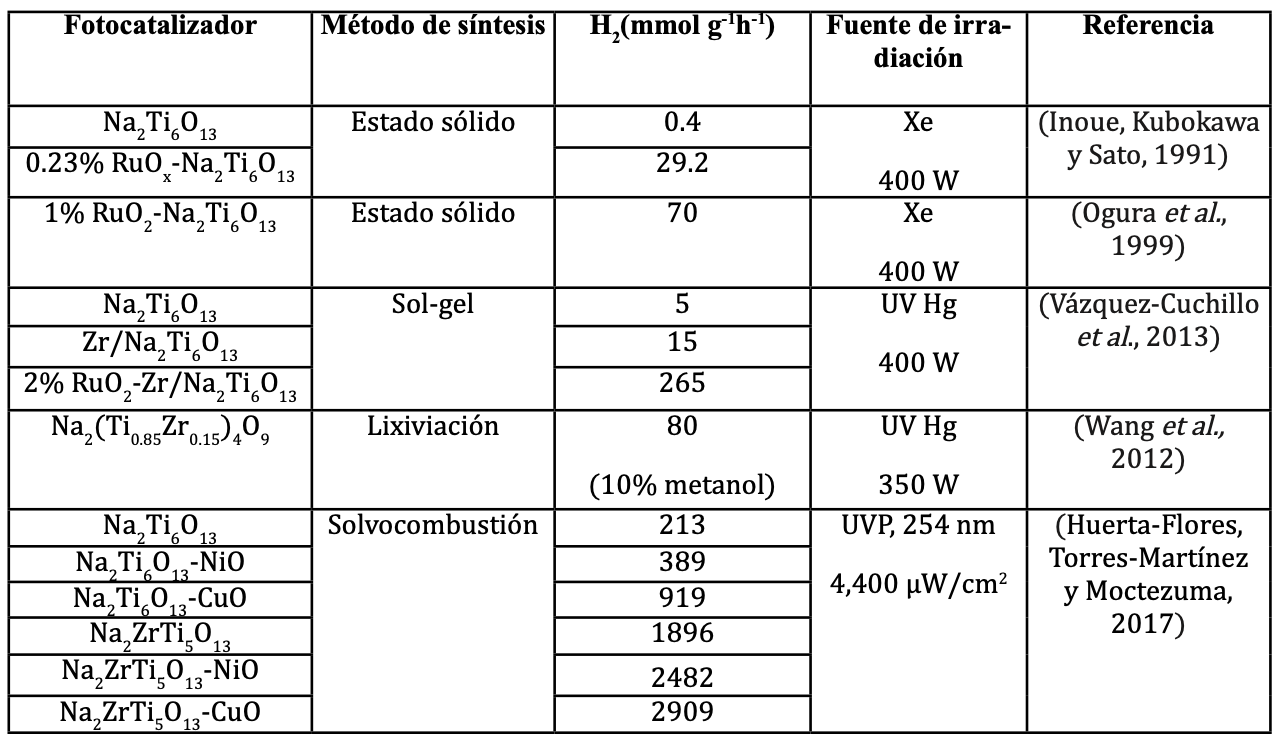
Tabla IV. Resumen de las actividades reportadas para la producción de hidrógeno en sistemas fotocatalíticos sobre las fases Na2Ti6O13 y Na2Ti5ZrO16.
CONCLUSIONES
- De la revisión de los artículos más recientes de investigaciones sobre la producción fotocatalítica de hidrógeno utilizando el NaTaO3 con estructura tipo perovskita y la solución sólida MO/Na2ZrxTi6-xO13 (x = 0,1), se puede concluir lo siguiente:
- Fue posible obtener películas delgadas altamente cristalinas de las fases NaTaO3 por la técnica de LCVD para su aplicación en la producción fotocatalítica de hidrógeno.
- Se demostró que la composición y microestructura de las películas se puede controlar a través de las condiciones de depósito.
- La técnica de LCVD permite la obtención de películas de diferente composición, estructura cristalina y microestructura.
- La actividad fotocatalítica para la producción de hidrógeno de la película de NaTaO3 ortorrómbico fue seis veces mayor a la de la película de NaTaO3 monoclínico.
- La actividad obtenida en la película de NaTaO3 ortorrómbico es 13 veces mayor a la mostrada por el mismo material en polvo obtenido por el método de solvocombustión. Esta actividad se relacionó directamente con la microestructura de tipo piramidal con la presencia de nanoescalones observada en el NaTaO3 ortorrómbico.
- Se demostró que la actividad fotocatalítica de los materiales preparados en este trabajo por LCVD en película delgada es altamente competitiva comparada con la de fotocatalizadores similares preparados por otros métodos, por lo que se recomienda el uso de estas técnicas para la fabricación de fotocatalizadores nanoestructurados para su uso en reactores a mayor escala.
- Se prepararon exitosamente las fases isoestructurales Na2ZrxTi6-xO13 (x = 0, 1) por los métodos de estado sólido, sol-gel y solvocombustión, obteniendo estructuras unidimensionales (1D).
- Los materiales exhibieron alta estabilidad para la producción de hidrógeno y oxígeno (en el material dopado con Zr) durante tres horas.
- El Na2ZrTi5O13 mostró la actividad más alta de producción de H2 (1896 μmolg-1h-1) comparando los demás titanatos. La incorporación de Zr4+ generó una distorsión en la estructura, lo cual mejoró el proceso de transporte y separación de cargas, redujo la recombinación e incrementó la actividad fotocatalítica.
- La morfología característica 1D del hexatitanato de sodio jugó un rol muy importante en la actividad fotocatalítica, incrementando la separación de las cargas a través de la estructura 1D.
- Los titanatos se modificaron con nanopartículas de óxidos metálicos, MO (M = Ni, Cu), por el método de impregnación. Esto promovió un mejor transporte de cargas y una mayor actividad fotocatalítica. La actividad más alta se obtuvo en la fase Na2ZrTi5O13 modificada con CuO (2909μmolg-1h-1), y corresponde a un incremento de 13.6 veces la actividad del semiconductor puro.
- Este incremento en la actividad fotocatalítica se atribuyó a la formación de una heteroestructura n-p entre el titanato (semiconductor tipo n) y el CuO (semiconductor tipo p) promoviendo la separación, transferencia y utilización de las cargas fotogeneradas en la reacción fotocatalítica. En resumen, los fotocatalizadores desarrollados en este trabajo presentaron actividades competitivas para la producción de hidrógeno comparados con materiales similares reportados en la literatura.
* Universidad Autónoma de Nuevo León.
Contacto: leticia.torresgr@uanl.edu.mx; lettorresg@yahoo.com
REFERENCIAS
Bartels, J.R., Pate, M.B., y Olson, N.K. (2010). An economic survey of hydrogen production from conventional and alternative energy sources. International Journal of Hydrogen Energy. 35:8371-8384.
Cesar, I., Sivula, K., Kay, A., et al. (2009). Influence of Feature Size, Film Thickness, and Silicon Doping on the Performance of Nanostructured Hematite Photoanodes for Solar Water Splitting. J. Phys. Chem. C. 113:772-782.
Eng, H.W., Barnes, P.W., Auer, B.M., et al. (2003). Investigations of the electronic structure of d0 transition metal oxides belonging to the perovskite family. J. Solid State Chem. 175(1):94-109.
Gómez-Solís, C., Ruiz Gómez, M.A., Torres-Martínez, L.M., et al. (2014). Facile solvocombustion synthesis of crystalline NaTaO3 and its photocatalytic performance for hydrogen production. Fuel. 130-221-227.
Huerta-Flores, A.M., Chen, J., Torres-Martínez, L.M., et al. (2017). Laser assisted chemical vapor deposition of nanostructured NaTaO3and SrTiO3 thinfilms for efficient photocatalytic hydrogen evolution. Fuel. 197: 174-185.
Huerta-Flores, A.M., Torres-Martínez, L.M., y Moctezuma, E. (2017). Overall photocatalytic water splitting on Na2ZrxTi6-xO13(x=0,1) nanobelts modified with metal oxide nanoparticles as cocatalysts. International Journal of Hydrogen Energy 42 ,14547-14559. ISSN: 0360-3199.
Inoue, Y., Kubokawa, T., y Sato, K.J. (1991). Photocatalytic activity of alkali-metal titanates combined with ruthenium in the decomposition of water. Phys. Chem. 95:4059-4063.
Jitputti, J., Pavasupree, S., Suzuki, Y., et al. (2006). Photocatalytic Hydrogen Evolution over Tantalate Photocatalysts. Solar Ener. Conver. 0974:CC09.
Kisch, H. (2015). Photocatalysis: Principles and Applications. Wiley-VCH.
Krol, R., y Parkinson, B.A. (2017). Perspectives on the photoelectrochemical storage of solar energy. MRS Ener. & Sust. 4:1-11.
Kudo, A. (2003). Photocatalyst Materials for Water Splitting. Catalysis Surv. 7(1):31-38.
Kumar, P., Sharma, P., Shrivastav, R., et al. (2011). Electrodeposited zirconium-doped α-Fe2O3 thin film for photoelectrochemical water splitting. Int. J. Hydrogen Energy. 36:2777-2784.
Li, F., Yang, H., Li, W., et al. (2018). Device Fabrication for Water Oxidation, Hydrogen Generation, and CO2 Reduction via Molecular Engineering. Joule. 2(1):36-60.
Lv, M., Sun, X., Wei, S., et al. (2017). Ultrathin Lanthanum Tantalate Perovskite Nanosheets Modified by Nitrogen Doping for Efficient Photocatalytic Water Splitting. ACS Nano. 11(11):11441-11448.
Ogura, S., Kohno, M., Sato, K., et al. (1999). Photocatalytic properties of M2Ti6O13 (M=Na, K, Rb, Cs) with rectangular tunnel and layer structures: Behavior of a surface radical produced by UV irradiation and photocatalytic activity for water decomposition. Phys. Chem. Chem. Phys. 1:179-183.
Osterloh, F.E. (2013). Inorganic nanostructures for photoelectrochemical and photocatalytic water splitting. Chem. Soc. Rev. 42:2294-2320.
Rodríguez-Torres, J., Gómez-Solís, C., Torres-Martínez, L.M., et al. (2017). Synthesis and characterization of Au-Pd/NaTaO3 multilayer films for photocatalytic hydrogen production. Journal of Photochemistry and Photobiology A: Chemistry. 332:208-214.
Takata, T., Pan, C., y Domen, K. (2015). Recent progress in oxynitride photocatalysts for visible-light-driven water splitting. Sci. Technol. Adv. Mater. 16:033506.
Torres-Martínez, L.M., R. Gómez, O. Vázquez-Cuchillo, et al. (2010). Enhanced photocatalytic water splitting hydrogen production on RuO2/La: NaTaO3 prepared by sol-gel method. Catalysis Communications. 12:268-272.
Van Winsen, J.E. (2013). Phys. Research Project University Amsterdam.
Vázquez-Cuchillo, O., Gómez, R., Cruz-López, A., et al. (2013). Improving Water Splitting Using RuO2-Zr/Na2Ti6O13 as a Photocatalyst. Photochem. And Photobiol. A: Chemistry. 266:6-11.
Voorzanger, J. (2012). VU University Amsertdam.
Wan, W., Zhang, R., Ma, M., et al. (2018). Monolithic aerogel photocatalysts: a review. J. Mater. Chem. A. 6:754-775.
Wang, D.J., Li, Z.H., An, Y.L., et al. (2012). Photocatalytic H2 evolution property of Zr-doped sodium titanate nanobelts prepared by dealloying of Ti-based metallic glassy powders. Shen J. Int. Conf. Photosynthesis Research for Sustanability. 37:8240-8248.
Winter, C.J. (2009). Hydrogen energydAbundant, efficient, clean: A debate overthe energy-system-of-change. Int J. Hydrogen Energy. 34:S1-S52.
Zeng, S., Kar, P., Thakur, U.K., et al. (2018). A review on photocatalytic CO2 reduction using perovskite oxide nanomaterials. Nanotechnol. 29:5-15.
Zhu, X., Zhang. F., Wang, M. et al. (2014). Facile synthesis, structure and visible light photocatalytic activity of recyclable ZnFe2O4/TiO2. Appl. Surf. Sci. 319:83-89.