LOS COMPUESTOS QUÍMICOS Y LOS SERES VIVOS: ¿CÓMO SE ORIGINA LA LUMINISCENCIA?
CIENCIA UANL / AÑO 25, No.115, septiembre-octubre 2022
JAZMÍN MARROQUÍN FLORES*, LUIS ENRIQUE ROMERO GUTIÉRREZ*,
RAÚL COLORADO PERALTA*, DELIA HERNÁNDEZ ROMERO*
PDF: Ejes_115
La luminiscencia es un fenómeno en el que una o varias moléculas poseen la capacidad de emitir luz después de excitar sus electrones a través de la absorción de radiación.
Se conocen dos tipos de luminiscencia que dependen de la duración de la misma; por un lado, la luminiscencia de corta duración, denominada fluorescencia, y por otro, la luminiscencia que permanece después de haberse suspendido la fuente de excitación, denominada fosforescencia. Sin embargo, no todas las moléculas poseen esta maravillosa propiedad, para ello es necesario que posean enlaces conjugados, es decir, enlaces simples y dobles alternados, volviéndolas fotoexcitables.
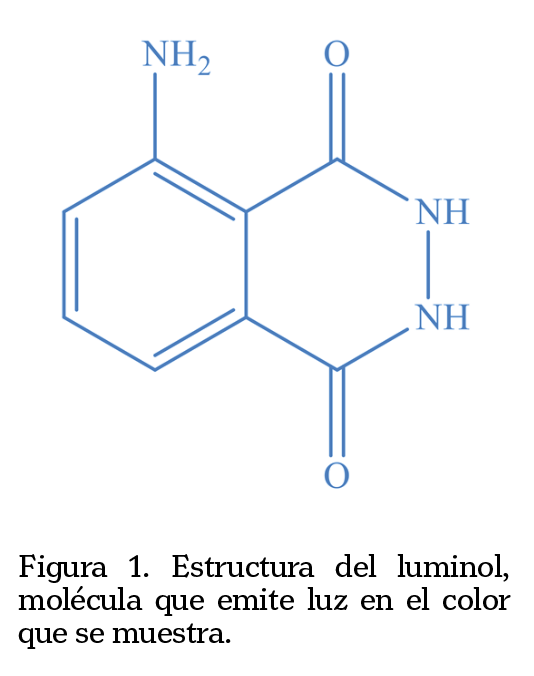
Las moléculas con enlaces dobles conjugados reciben el nombre de cromóforos (figura 1). Esta luz, o luminiscencia, contrario al tipo de luz que observamos en nuestros hogares, oficinas y autos, tiene la característica de no producir calor, por lo que suele considerarse como “luz fría” y se puede observar en diferentes tonalidades de color de acuerdo con la longitud de onda en que se esté excitando y a la que la molécula emita.
Es importante tener presente que en una molécula o material existen diversas fuentes para propiciar la emisión de luz, por ejemplo, es posible utilizar un campo eléctrico (electroluminiscencia) o un campo magnético (magnetoluminiscencia); por otro lado, si se utiliza ultrasonido (sonoluminiscencia), o bien si se utiliza calor (incandescencia), cuando se utilizan fotones (fotoluminiscencia) y cuando la luminiscencia se produce mediante una reacción química (quimioluminiscencia). Siendo estas dos últimas las más comunes (Báez-Rodríguez et al., 2019).
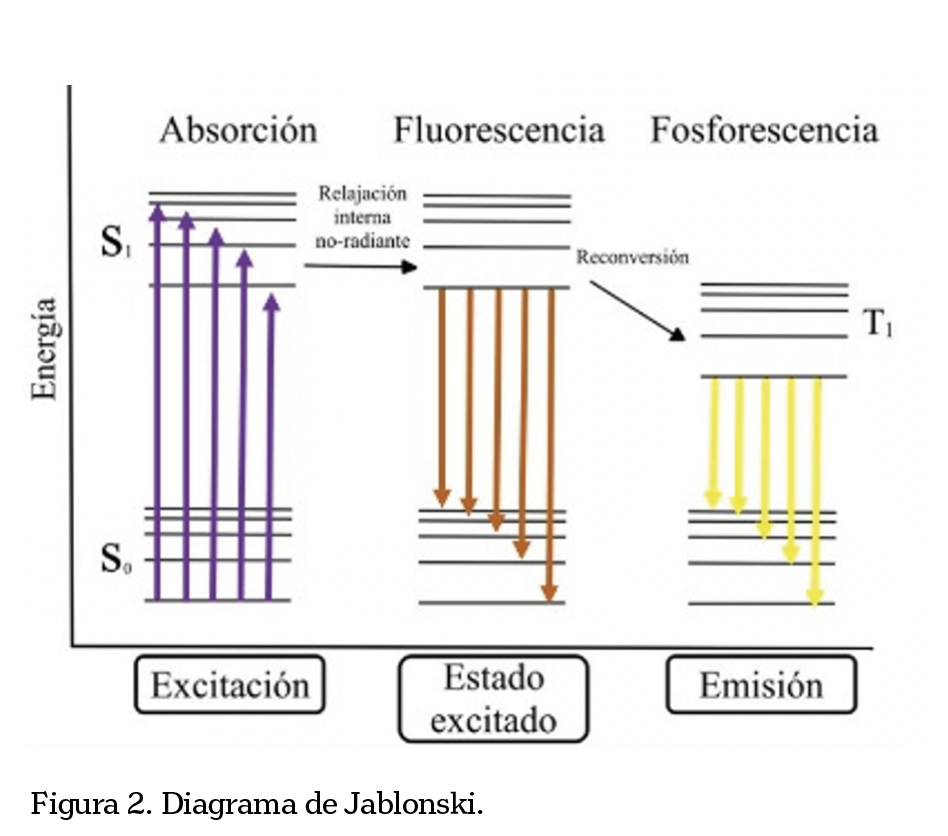
En el proceso de la luminiscencia existen tres etapas importantes: la excitación de la molécula (donde la fuente de energía puede ser diversa, como se mencionó anteriormente); la absorción de energía por parte de la molécula y, finalmente, la emisión de energía en forma de luz. En este sentido se puede hacer uso del conocido diagrama de Jablonski para explicar las etapas y los procesos de migración de energía en dicho fenómeno (figura 2).
En la primera etapa, la molécula es irradiada (excitada) por una fuente externa y ésta absorbe la energía, llevándola de un estado de menor energía a un estado excitado (de mayor energía); en la segunda etapa la molécula se encuentra en un estado excitado, el cual dura poco tiempo debido a que éstos tienden a volverse estados de relajación, ocasionando que la energía absorbida se disipe parcialmente (fluorescencia); finalmente, durante la última etapa la energía del fotón previamente absorbido es emitida después de un cruce entre sistemas (fosforescencia) (González-Roldan et al., 2015).
BIOLUMINISCENCIA
La naturaleza en muchas ocasiones nos permite disfrutar de espectáculos visuales asombrosos, como las auroras boreales, los arcoíris, las estrellas, la luz que se observa en las tormentas eléctricas, etcétera. Sin embargo, algunos organismos vivos también son protagonistas de su propio espectáculo visual, gracias a que poseen la capacidad de producir luz a voluntad, la cual es aprovechada para distintos propósitos, por ejemplo, como medio de defensa o reproducción. En estos casos es muy común cometer el error de referirnos a estos organismos como “organismos brillantes”, y lo que realmente está ocurriendo en ellos es una serie de reacciones en las que se libera energía que podemos apreciar en forma de luz.
Esta habilidad de los seres vivos para producir luz propia ocurre de dos maneras principalmente: (1) cuando se origina por la presencia de moléculas fotoexcitables, que absorben luz a una determinada longitud de onda, y en consecuencia la emiten a una distinta longitud de onda a la que fue absorbida (fotoluminiscencia); o bien, (2) puede ocurrir mediante quimioluminiscencia, un fenómeno causado por la interacción de la luciferasa (enzima que facilita la reacción) y la luciferina, que en presencia de oxígeno ocasionan la emisión de energía en forma de luz. Este fenómeno ocurre cuando la luciferina es oxidada por el oxígeno, en donde es esencial la presencia de la luciferasa para acelerar la reacción y una molécula de ATP (adenosín trifosfato), el cual proporciona la energía necesaria. Los organismos bioluminiscentes pueden producir luz azul, verde o en algunos casos de color rojo (Haddock, et al., 2009).
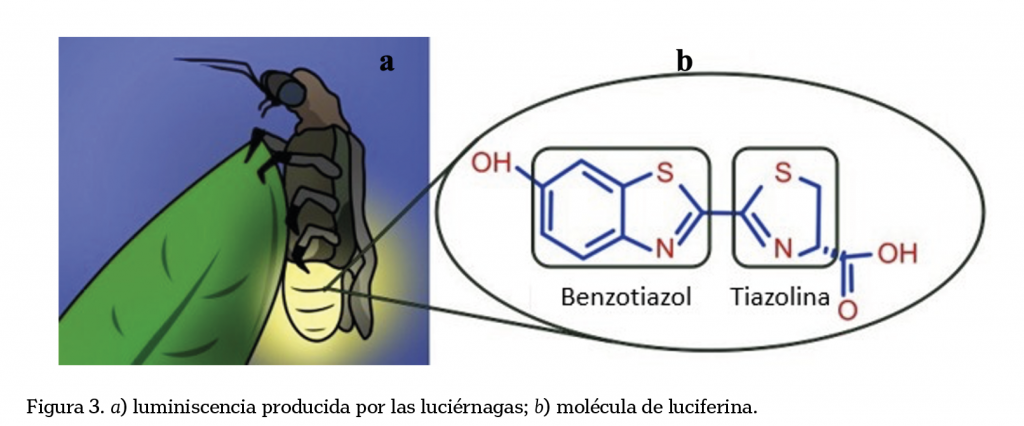
La luciferina es un compuesto heterocíclico, es decir, una molécula que posee un sistema de anillos en los que un átomo distinto al carbono puede estar presente (como nitrógeno, oxígeno o azufre). La luciferina posee en su estructura un anillo de tiazolina y otro de benzotiazol (figura 3b); podría decirse que el lado del anillo de la tiazolina es la parte más activa de la molécula, puesto que éste es el fragmento que interactúa con la luciferasa, para la posterior producción o emisión de bioluminiscencia. Hasta hace algún tiempo, el caso de las luciérnagas (figura 3a) era el más conocido; sin embargo, es bien sabido que hay muchos más organismos capaces de producir su propia luz (Meighen, 1991).
Aunque algunos organismos terrestres, como las luciérnagas, larvas y algunos hongos son ejemplos de organismos bioluminiscentes, la bioluminiscencia es observable principalmente en organismos de ambiente marino, por ejemplo, ctenóforos, sinofóros, dinoflagelados y algunas bacterias (Meighen, 1991; Haddock, et al., 2009). Estos organismos marinos poseen la capacidad de iluminar algunas partes de su cuerpo de manera controlada e incluso modular la intensidad de la luz que emiten.
Como ya se mencionó, es más común observar organismos marinos luminiscentes, pero ¿cuál es el propósito de producir esta luz? Resulta interesante que los organismos que habitan en zonas no profundas con abundante luz han desarrollado cuerpos translúcidos para evadir a sus depredadores, y algunos otros permanecen en zonas más profundas durante el día para evitar ser vistos. En este sentido, si algunos organismos buscan ocultarse, ¿por qué producir luz si ésta los puede poner a la vista de sus depredadores?, se sabe que la mayoría de estos organismos recurren a la luminiscencia como mecanismo de defensa, para simular la luz procedente de la superficie y de esta manera ocultarse, o bien asustar a sus depredadores, distrayéndolos mientras huyen o simplemente atraer al depredador del organismo que atente contra su integridad (Bioluminiscencia, 2016).
COMPUESTOS LUMINISCENTES
Si bien la luminiscencia es un fenómeno natural, que se observa en ciertos organismos, en el laboratorio también es posible obtener compuestos químicos que presenten dicha propiedad, por lo que el diseño y síntesis de moléculas que posean esta característica es una labor de interés para los químicos orgánicos e inorgánicos. En la bibliografía mucho se ha mencionado de la obtención de compuestos luminiscentes, por lo que en esta parte nos centraremos en los compuestos de coordinación con iones lantánidos, ya que durante las últimas décadas ha tenido gran impacto, debido a las diversas áreas en las que se pueden aplicar, por ejemplo, tienen importancia tecnológica en la fabricación de materiales ópticos y magnéticos, así como para catálisis y aditivos, en la industria metalúrgica (Bünzli, 2006).
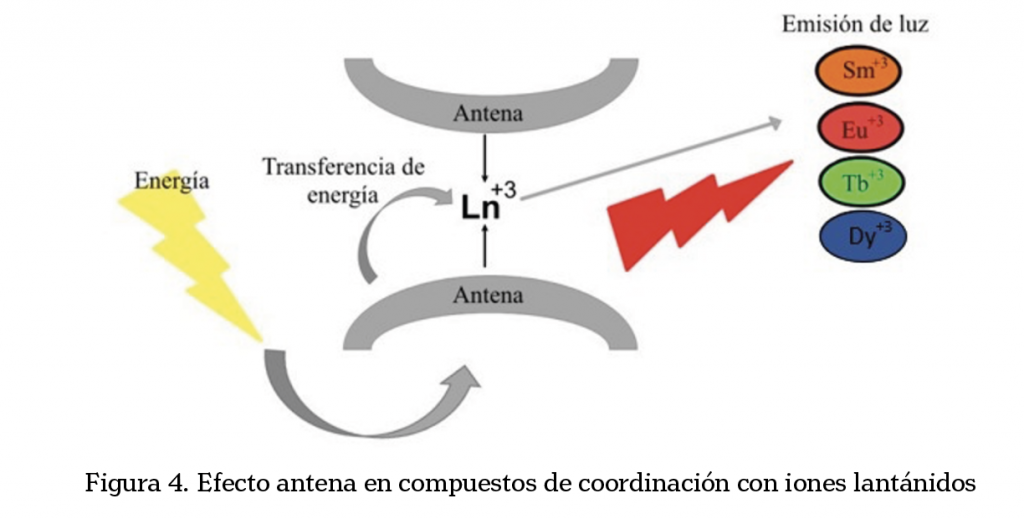
Un compuesto de coordinación está constituido básicamente por dos partes importantes: una molécula orgánica o cromóforo (mejor conocido como ligante) y un metal, en donde el metal se encuentra “secuestrado” mediante enlaces de coordinación proveniente de la parte orgánica. La eficiencia en la luminiscencia en este tipo de compuestos depende, en gran parte, de la capacidad del ligante para absorber la energía que se le suministre (Chang y Goldsby, 2013). Mientras más ricos en electrones π conjugados sean los ligantes (electrones propios de un doble enlace), más eficiente será la transferencia de energía al metal. Éste es un proceso mejor conocido como “efecto antena” y es muy característico en los compuestos de coordinación obtenidos con metales de transición interna (lantánidos) (figura 4).
En este caso las transiciones electrónicas responsables de la luminiscencia son muy débiles y por lo tanto es muy difícil observarla. Cuando una molécula orgánica se comporta como una buena “antena” y absorbe de manera eficiente la energía, ésta tiene la capacidad de transferirla al centro metálico, favoreciendo de esta manera la estimulación de las transiciones electrónicas del metal, se dice entonces que “se sensibiliza la luminiscencia”, ocasionando la emisión de luz.
Los lantánidos presentan transiciones electrónicas muy características para cada núcleo atómico, dichas transiciones se observan a diferentes longitudes de onda, yendo desde el UV-Visible (Gd³⁺, Tm³⁺, Tb³⁺, Sm³⁺ y Eu³⁺) hasta el infrarrojo cercano (Pr³⁺, Nd³⁺, Er³⁺ y Yb³⁺), por lo que resulta interesante observar diferentes colores, por ejemplo, el ion Sm³⁺ produce un color anaranjado, mientras que el ion Eu³⁺ un color rojo, y el ion Tb³⁺ un color verde muy característico (figura 5). Como resultado de estas transiciones electrónicas, algunos de los lantánidos presentan luminiscencia, por un lado, los iones Pr³⁺ (praseodimio), Nd³⁺ (neodimio), Ho³⁺ (holmio), Er³⁺ (erbio) y Yb³⁺ (iterbio) presentan fluorescencia, mientras que los iones Sm³⁺ (samario), Eu³⁺ (europio), Gd³⁺ (gadolinio), Tb³⁺ (terbio), Dy³⁺ (disprosio) y Tm³⁺ (tulio) presentan fosforescencia (Uh y Petoud, 2010).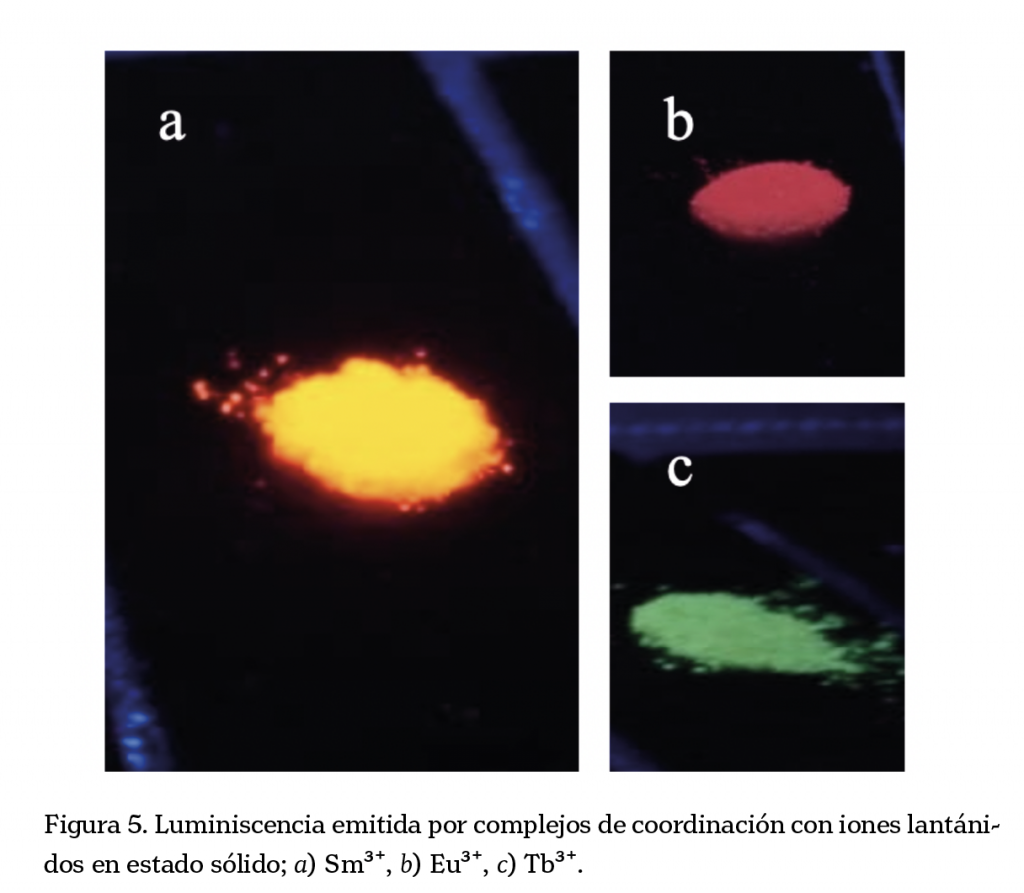
CONCLUSIONES
La obtención y estudio de compuestos luminiscentes (ya sean sintéticos o naturales) es de gran importancia, pues se les puede dar diversas aplicaciones, por ejemplo, existen reportes sobre el uso de compuestos de coordinación con lantánidos y otros metales para su uso como biomarcadores por su gran luminiscencia. En el ámbito de la óptica, se ha mencionado que pueden utilizarse como diodos orgánicos emisores de luz (OLED´s) o bien en tintas de seguridad.
*Universidad Veracruzana, Orizaba, México.
Contacto: deliahernandez@uv.mx
REFERENCIAS
Báez-Rodríguez, A., Zamora-Peredo, L., García-González, L., et al. (2019). Luminescent materials: natural and synthetic. Materia, Ciencia y Nanociencia. 2(1):21-30.
Bünzli, J.C.G. (2006). Benefiting from the unique properties of lanthanide ions. Accounts of Chemical Research. 39(1):53-61. Doi:10.1021/ar0400894
Chang,R., y Goldsby, K.A. (2017). Química. México: Mc Graw Hill/Interamericana Editores.
González Rodal, D., Godino Ojer, M., Smuszkiewicz, Á., et al. (2015). Técnicas luminiscentes en criminalística. Revista 100cias@ uned. 8:76-82.
Haddock, S.H., Moline, M.A., y Case, J.F. (2009). Bioluminescence in the sea. Annual Review of Marine Science. 2:443-493. Doi:10.1146/annurev-marine-120308-081028
Meighen, E.A. (1991). Molecular biology of bacterial bioluminescence. Microbiology and Molecular Biology Reviews. 55(1):123-142. Doi:0146-0749/91/010123-20$02.00/0
Uh, H., y Petoud S. (2010). Novel antennae for the sensitization of near infrared luminescent lanthanide cations. Comptes Rendus Chimie. 13(6-7):668–680. Doi:10.1016/j.crci.2010.05.007
National Geographic. (2016). Bioluminiscencia. Una de las principales fuentes de luz del planeta son los seres vivos. National Geographic España. Disponible en: https://www.nationalgeographic.com.es/ciencia/grandes-reportajes/bioluminiscencia-2_8954